PAU Química Catalunya (2001-2023)
Termodinàmica química
PAU 2023 sèrie 2 problema 2
Enunciat

Pauta

PAU 2023 sèrie 5 problema 3
Enunciat

Pauta

PAU 2023 sèrie 1 problema 1
Enunciat

Pauta

PAU 2022 sèrie 3 problema 1
Enunciat

Pauta

PAU 2022 sèrie 5 problema 3
Enunciat

Pauta

PAU 2022 sèrie 2 problema 3
Enunciat

Pauta

PAU 2021 sèrie 1 problema 6
Enunciat

Pauta

PAU 2021 sèrie 2 problema 2
Enunciat

Pauta
PAU 2021 sèrie 2 problema 6
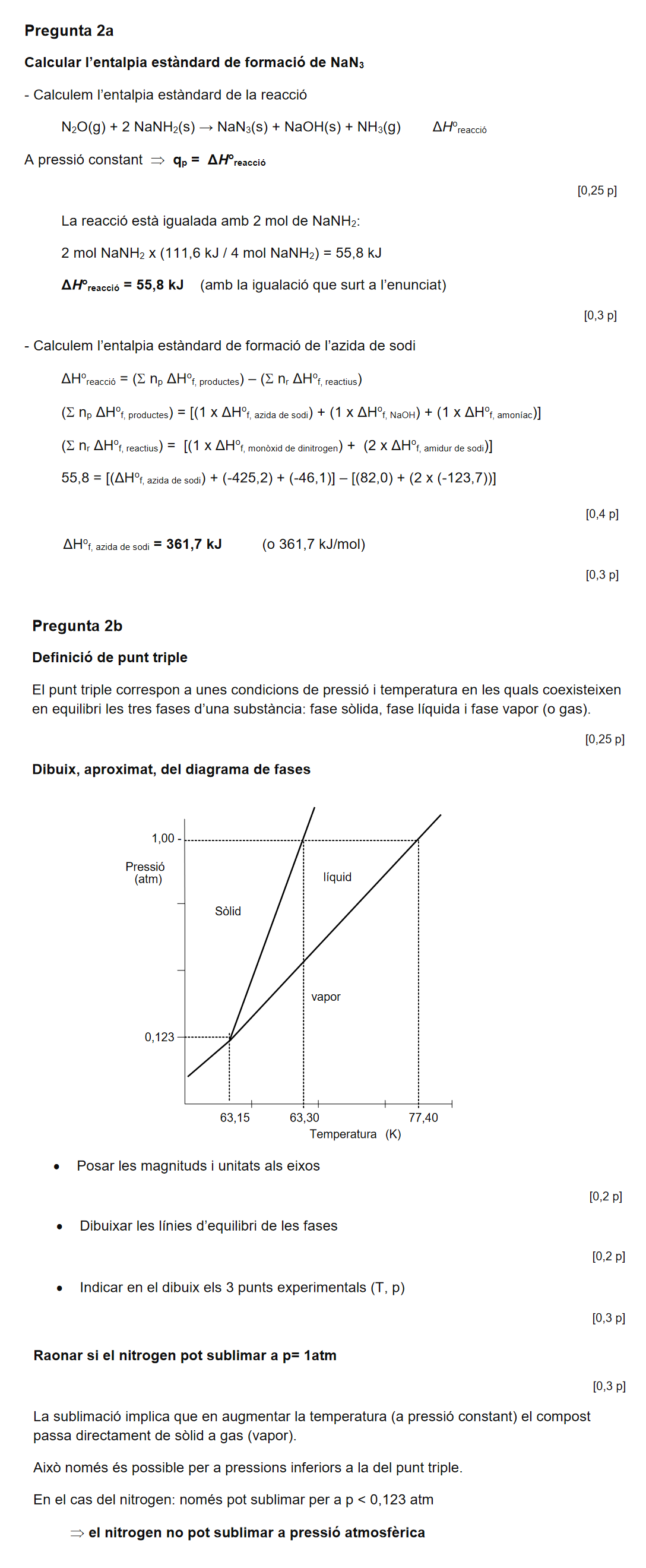
Enunciat

Pauta

PAU 2021 sèrie 5 problema 7
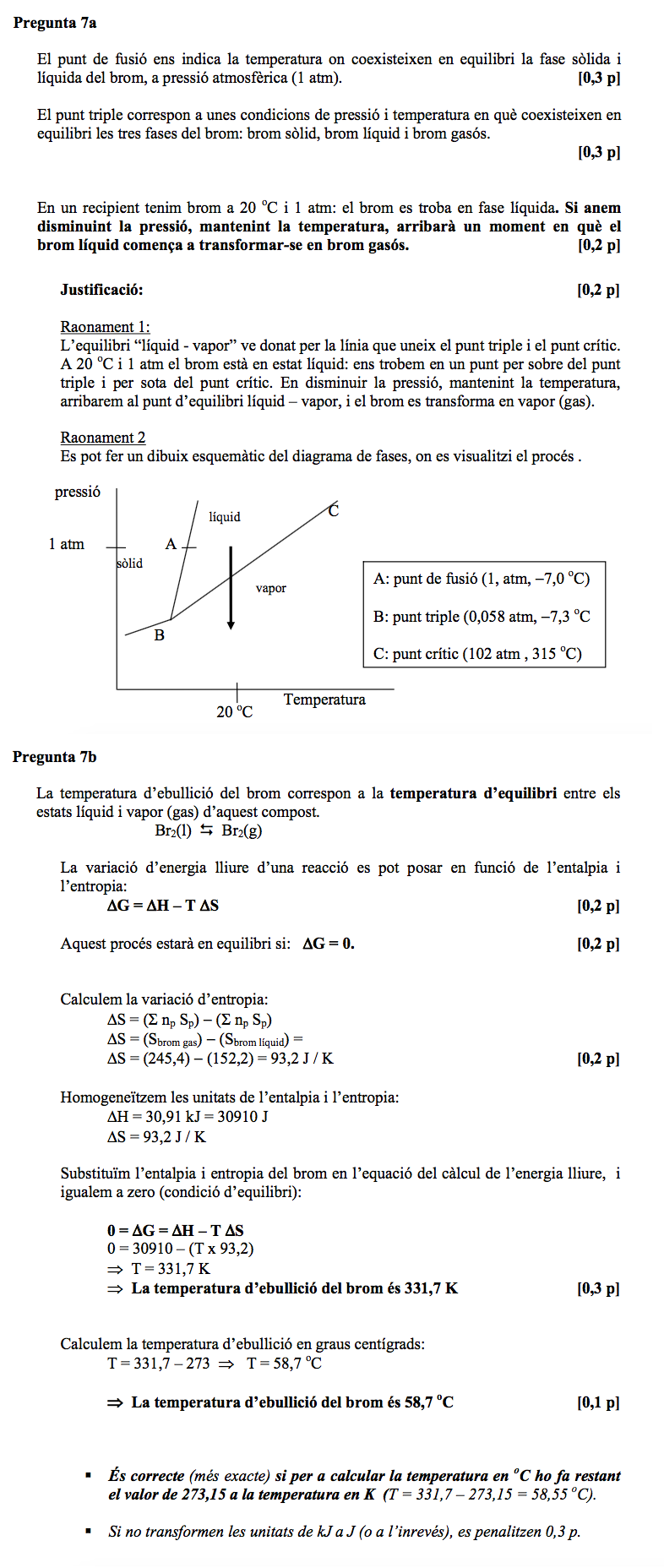
Enunciat

Pauta

PAU 2020 sèrie 1 problema 3
Enunciat

Pauta

PAU 2020 sèrie 3 problema 5
Enunciat

Pauta

PAU 2019 sèrie 5 problema 6
Enunciat

Pauta

PAU 2019 sèrie 5 problema 1
Enunciat

Pauta

PAU 2019 sèrie 4 problema 6
Enunciat

Pauta

PAU 2019 sèrie 4 problema 1
Enunciat

Pauta

PAU 2019 sèrie 1 problema 3
Enunciat

Pauta

PAU 2018 sèrie 3 problema 6
Enunciat
Pauta
PAU 2018 sèrie 5 problema 6
Enunciat
Pauta
PAU 2018 sèrie 1 problema 3
Enunciat

Pauta

PAU 2018 sèrie 1 problema 7
Enunciat

Pauta

PAU 2017 sèrie 2 problema 1
Enunciat

Pauta

PAU 2017 sèrie 5 problema 4
Enunciat

Pauta

PAU 2017 sèrie 1 problema 1
Enunciat

Pauta

PAU 2016 sèrie 1 problema 4
Enunciat

Pauta

PAU 2016 sèrie 5 problema 5
Enunciat
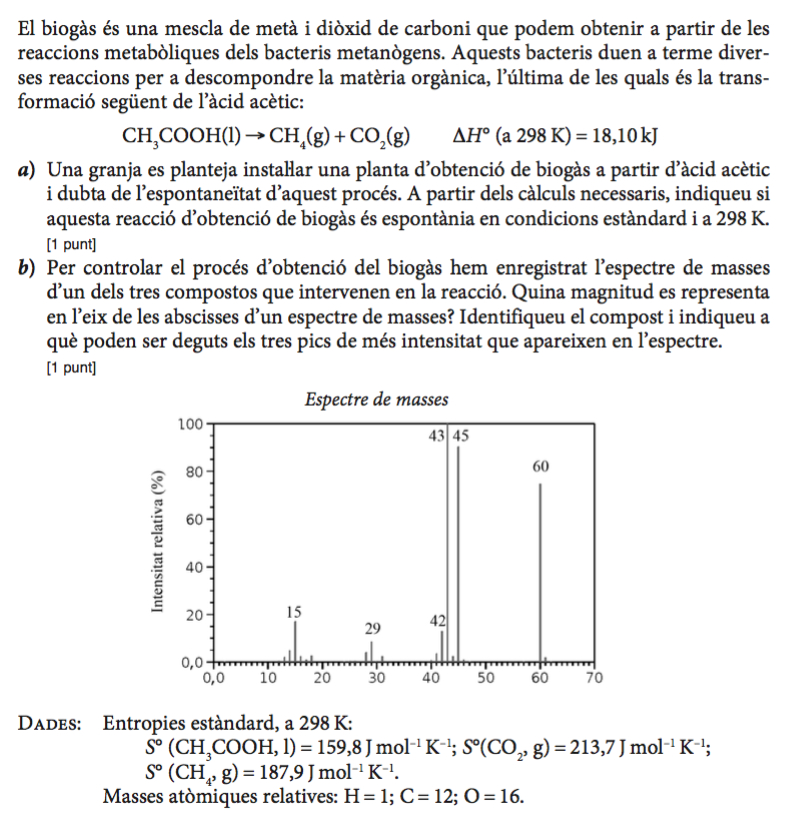
Pauta

PAU 2016 sèrie 5 problema 4
Enunciat

Pauta

PAU 2015 sèrie 5 problema 2
Enunciat

Pauta

PAU 2015 sèrie 4 problema 2
Enunciat

Pauta

PAU 2015 sèrie 2 problema 7
Enunciat

Pauta
PAU 2015 sèrie 2 problema 5
Enunciat
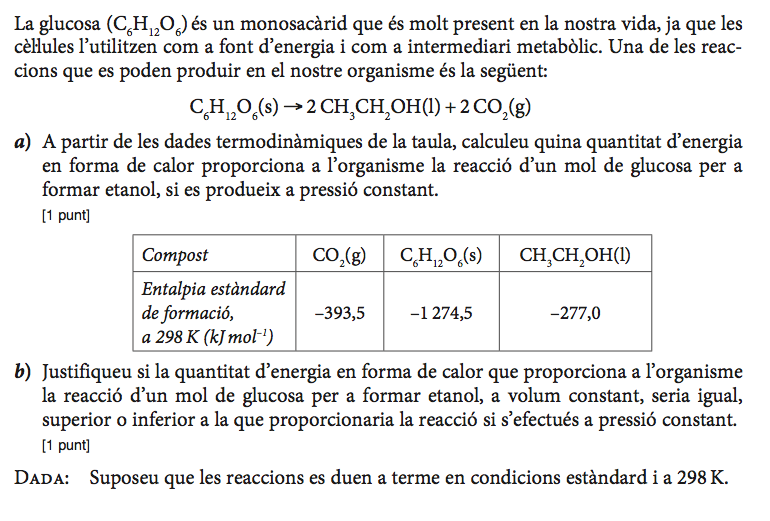
Pauta

PAU 2014 sèrie 5 problema 3
Enunciat

Pauta

PAU 2014 sèrie 4 problema 4
Enunciat

Pauta

PAU 2014 sèrie 3 problema 3
Enunciat

Pauta

PAU 2013 sèrie 1 problema 3
Enunciat

Pauta

PAU 2013 sèrie 3 problema 1
Enunciat
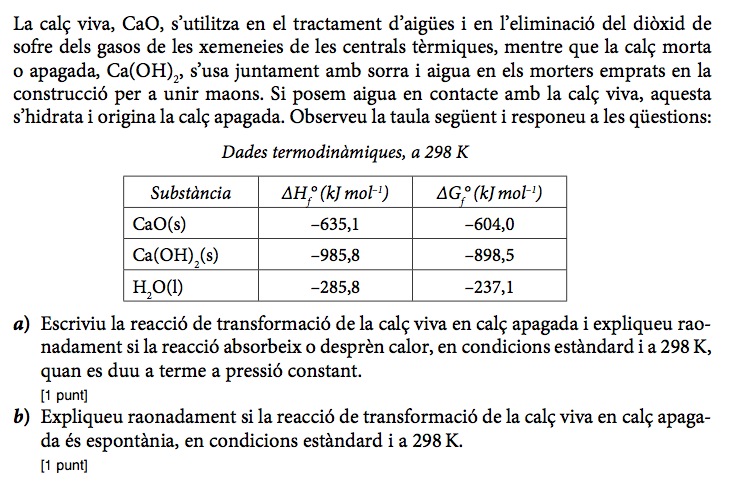
Pauta

PAU 2013 sèrie 4 problema 1
Enunciat

Pauta

PAU 2012 sèrie 4 problema 2
Enunciat

Pauta

PAU 2012 sèrie 1 problema 5
Enunciat

Pauta

PAU 2012 sèrie 3 problema 7
Enunciat
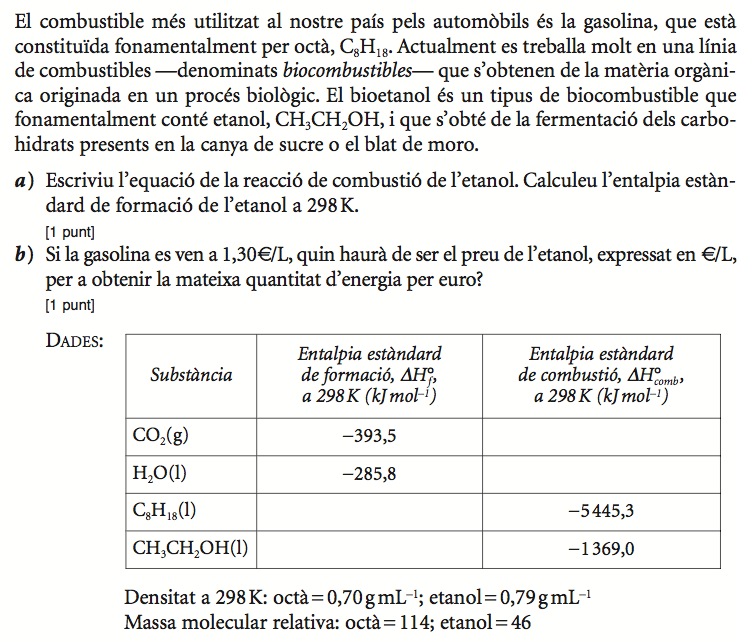
Pauta

PAU 2012 sèrie 3 problema 3
Enunciat

Pauta

PAU 2011 sèrie 2 problema 5
Enunciat

Pauta

PAU 2011 sèrie 4 problema 2
Enunciat

Pauta

PAU 2011 sèrie 4 problema 4
Enunciat

Pauta

PAU 2011 sèrie 1 problema 4
Enunciat

Pauta

PAU 2011 model d'exercici 7
Enunciat
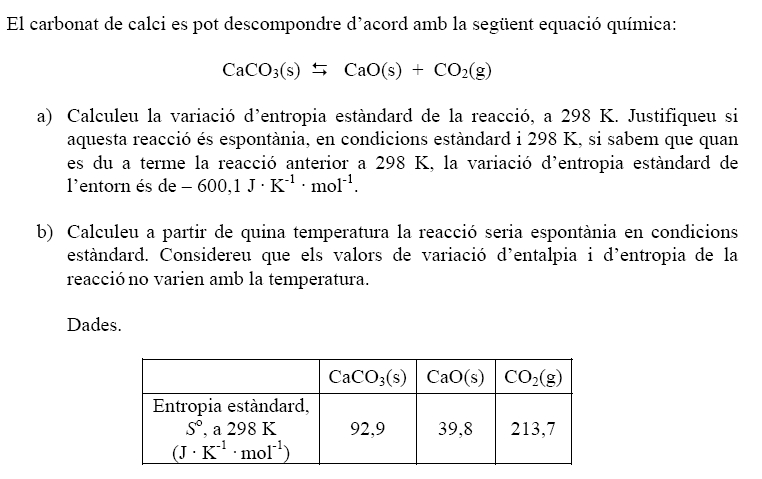
Pauta

PAU 2010 sèrie 2 problema 7
Enunciat

Pauta

PAU 2010 sèrie 2 problema 6
Enunciat

Pauta

PAU 2010 sèrie 2 problema 3
Enunciat

Pauta

PAU 2010 sèrie 4 problema 5
Enunciat

Pauta

PAU 2010 sèrie 4 problema 3
Enunciat

Pauta

PAU 2010 sèrie 1 problema 2
Enunciat

Pauta

PAU 2009 sèrie 1 problema 1
Enunciat

Pauta

PAU 2009 sèrie 3 problema 1
Enunciat

Pauta

PAU 2009 sèrie 4 problema 1
Enunciat

Pauta

PAU 2008 sèrie 5 problema 3
Enunciat

Pauta

PAU 2008 sèrie 4 opció B problema 4
Enunciat

Pauta

PAU 2008 sèrie 2 problema 1
Enunciat

Pauta

PAU 2007 sèrie 3 opció A problema 5
Enunciat

Pauta

PAU 2007 sèrie 3 problema 1
Enunciat

Pauta

PAU 2007 sèrie 2 problema 1
Enunciat

Pauta

PAU 2007 sèrie 1 opció A problema 4
Enunciat

Pauta
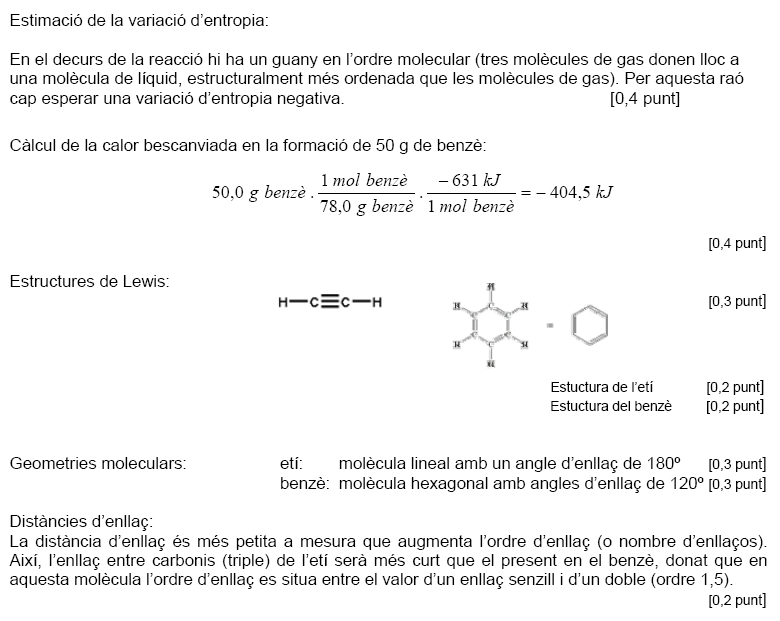
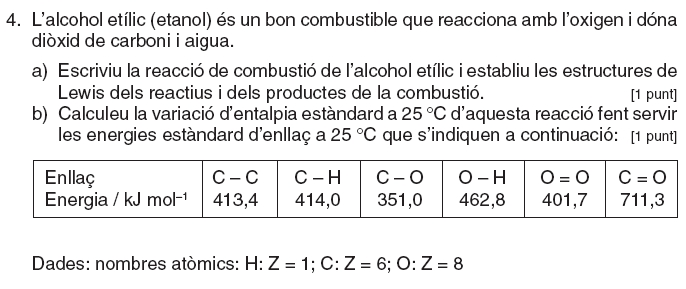
PAU 2006 sèrie 4 opció B problema 4
Enunciat
Pauta
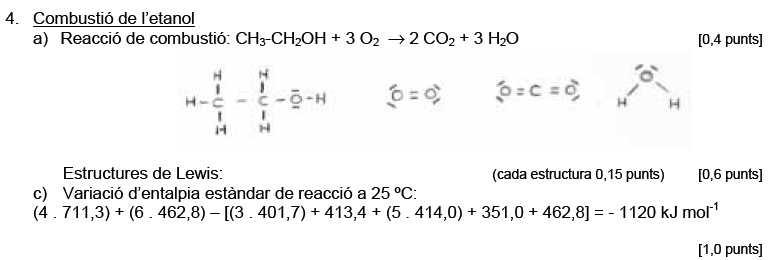
PAU 2006 sèrie 3 opció A problema 4
Enunciat

Pauta

PAU 2005 sèrie 4 problema 3
Enunciat

Pauta

PAU 2005 sèrie 3 opció B problema 4
Enunciat

Pauta
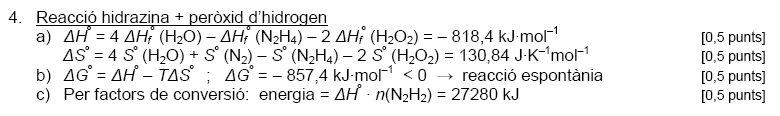
PAU 2004 sèrie 5 problema 2
Enunciat

Pauta
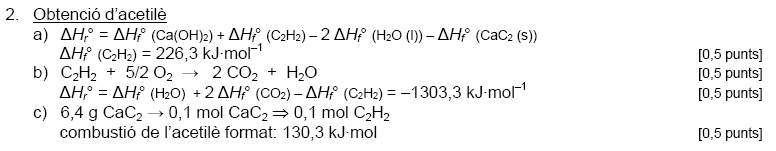
PAU 2004 sèrie 3 problema 2
Enunciat

Pauta

PAU 2004 sèrie 1 opció A problema 5
Enunciat
Pauta

PAU 2003 sèrie 5 problema 2
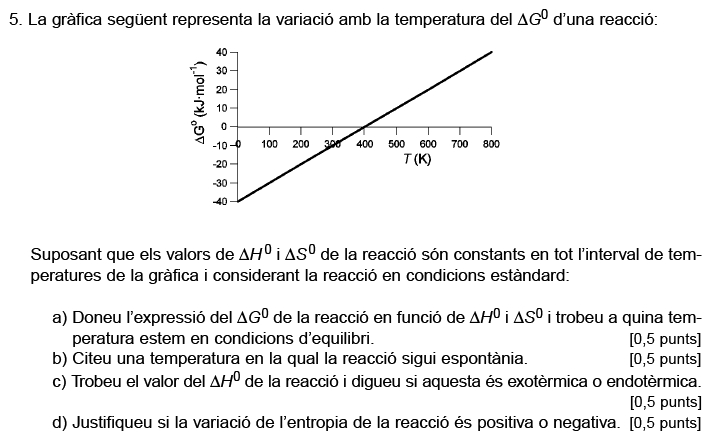
Enunciat

Pauta

PAU 2002 sèrie 2 problema 2
Enunciat

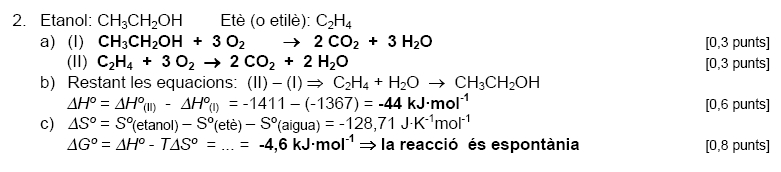
Pauta
PAU 2002 sèrie 3 opció A problema 5
Enunciat

Pauta

PAU 2001 sèrie 5 opció A problema 5
Enunciat

Pauta
Pauta no disponible.
PAU 2001 sèrie 4 opció B problema 5
Enunciat

Pauta

PAU 2001 sèrie 2 problema 3
Enunciat

Pauta
